1. Qué son los gases de combustión
1.1 Unidades de medición
La
presencia de contaminantes en los gases de combusti6n puede detectarse a partir
de ]a concentraci6n de los compuestos del gas. Generalmente, se utilizan las
unidades siguientes:
ppm
(partes por millón)
Corno
" el tanto por ciento (%)" ppm describe una proporción. Por ciento
significa "un número x de partes de cada cien", mientras que ppm
significa "un número x de partes en cada millón". Por ejemplo, si en
un cilindro de gas hay 250 ppm de mon6xido de carbono (C0), entonces, si
partimos de un mi116n de partículas de gas, 250 son de mon6xido de carbono. Las
otras 999.750 partículas son de nitrógeno (N2) y de oxigeno(02 ). La unidad ppm
es independiente de la presión y la temperatura, y se utiliza en concentraciones
bajas. Si la concentraci6n presente es elevada, se expresa en porcentaje (%). La
conversi6n es como sigue:
| 10 000 ppm | = | 1
|
| 1 000 ppm | = | 0.1% |
| 100 ppm | = | 0.01% |
| 10 ppm | = | 0.001% |
| 1 ppm | = | 0.0001% |
Ejemplo:
Una
concentraci6n de oxígeno del 21 ,, es equivalente a una concentraci6n de 210.000
ppm 02.
mg/Nm3
(miligramos por metro cúbico)
Con
la unidad mg/Nm 3, el volúmen normal (normal metros cúbicos, Nm3) se toma como
una variable de referencia y la masa del gas que poluciona se indica en
miligramos (mg). Como esta
unidad
varia con la presión y la temperatura, se toma como referencia el volúmen en
condiciones normales. Las condiciones normales son como siguen:
| Temperatura: | 0 şC |
| Presión: | 1013 mbar (hPa) |
De todas formas, esta informaci6n por si sola no es suficiente, ya que los volúmenes
Conversiones
a mg/Nm3
| CO (mg/m3) | = | |
| NOx (mg/m3) | = |
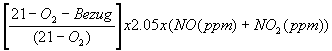
|
| SO2 (mg/m3) | = |
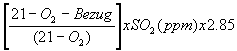
|
Los
factores en
]a f6rmula corresponden a una densidad estándar de los gases en mg/m3.
mg/kWh
(miligramos por kilowatio hora de energía)
| Gasoil EL | ||
| CO | 1 ppm = 1.110 mg/kWh | 1 mglkWh = 0.900 ppm |
| 1 Mg/M3 = 0.889 mg/kWh | 1 mg/kWh = 1.125 mg/m3 | |
| NOx | 1 ppm = 1.822 mg/kWh | 1 mg/kWh = 0.549 ppm |
| 1 mg/m3 = 0.889 mg/kWh | 1 mg/kWh = 1.125 mg/m3 | |
|
Gas Natural H (G 20) |
||
| CO | 1 ppm = 1.074 mg/kWh | 1 mg/kWh = 0.931 ppm |
|
1
Mg/M3 = |
1 mg/kWh = 1.164 Mg/M3 | |
| NOx | 1 ppm = 1.759 mglkWh | 1 mg/kWh = 0.569 ppm |
| 1 mg/ml = 0.859 mg/kWh | 1 mg/kWh = 1.164 rng/m3 | |
1.2
Componentes
de los gases de combustión
Los
componentes de los gases de combustión se listan más adelante ordenadas según
la concentración en el gas.
Los
factores de conversión para combustibles sólidos también dependen de la forma
en que estos están disponibles (en una pieza, como gravilla, polvo, fragmento,
etc.). Por ello los factores deben chequearse cuidadosamente.
Nitrógeno (N2)
El
nitrógeno (N2) es el principal componente (79 % vol.) del aire que
respiramos. Este gas
Valores
típicos en gases de combustión: Calderas gas/gasoil: 78 % - 80 %
El dióxido de carbono es un gas incoloro, inodoro con un ligero sabor agrio. Bajo la influencia de la luz solar y el verde de las hojas, clorofila, las plantas convierten el dióxido de carbono (CO2) en oxigeno (O2) . La respiración humana y animal convierten el oxígeno (O2) otra vez en di6xido de carbono (CO2) . Esto crea un equilibrio que los productos gaseosos de la combusti6n distorsionan. Esta distorsi6n acelera el efecto invernadero. El valor limite de efecto es de 5.000 ppm. A concentraciones superiores al 15% en volúmen (150.000 ppm) en la respiración, se produce una pérdida inmediata de conciencia.
Valores
típicos en gases de combustión..
Calderas de
gasoil.. 12.5 % - 14 % /
Calderas de gas 10% - 12%.
Oxígeno (O2)
Parte del oxigeno (0,) disuelto en el aire combina con el hidrógeno (H 2 ) del combustible y forma agua (H20). Según la temperatura de los gases de combusti6n (TH), esta agua se convierte en humedad del gas o en condensados. El oxigeno restante nos sirve para medir el rendimiento de la combusti6n y se utiliza para determinar las pérdidas por chimenea y el contenido de di6xido de carbono (CO,).
Valores típicos en gases de combustión:
Calderas de gasoil: 2 % - 5 %
Calderas de gas: 2 % . 3 %.
El monóxido de carbono es un gas venenoso al respirar, incoloro, inodoro y es el producto de una combusti6n incompleta. En una concentraci6n demasiado elevada, no permite que la sangre absorba oxigeno. Si, por ejemplo, el aire de una habitaci6n contiene 700 ppm CO, una persona respirando durante 3 horas morir. El valor límite de efecto es de 50 ppm.
Valores
típicos en gases de
combustión:
Caldera
de gasoil:
80 ppm -
150 ppm
Caldera
de
gas: 80
ppm
- 100
ppm.
Óxidos de nitrógeno (NOx)
A
altas temperaturas (combustión), el nitrógeno (N2) presente en el
combustible y en el aire ambiente combina con el oxigeno del aire (O2)
y forma mon6xido de nitr6geno (NO).
Valores típicos en gases de combustión:
Calderas
gas / gasoil: 50 ppm - 100 ppm
El
dióxido de azufre (S02 ) es un gas t6xico, incoloro con un olor fuerte. Se
forma a partir del azufre del combustible. El valor limite del efecto es de 5
ppm. E] Ácido sulfúrico (H2SO2) se forma en combinación
con el agua (H20) o condensados.. Valores típicos en gases de combustón
de calderas de gasoil: 180 ppm -
220 ppm.
Hidrocarburos inquemados (CxHy)
Los
hidrocarburos inquemados (C,H ) se forman cuando la combusti6n es incompleta y
contribuyen al efecto invernadero. Este grupo incluye metano (CH,), butano (C,Hlo)
y benzeno.(C6 H d' Valores típicos
en gases de combustión
de calderas de gasoil: <50 ppm.
Hollín
El
hollín también es carbón puro,
resultante de una combustión incompleta. Valores típicos
en gases de combustión
de calderas de gasoil.. HoWn derivado
0 6 1.
Partículas
sólidas
Las
partículas sólidas (polvo) es el nombre que se da a pequeńas partículas sólidas
distribuidas en el aire. Esto puede ocurrir en cualquier forma y densidad. Se
forman a partir de ]as cenizas y de los minerales que componen los combustibles
sólidos.